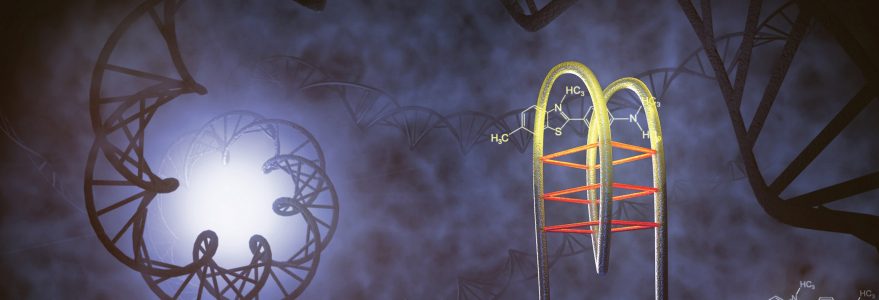
Fizycy z Laboratorium Procesów Ultraszybkich UW pokazali, jak wykryć zmiany w strukturze DNA, które mogą być przyczyną chorób genetycznych. Wykorzystali do tego barwnik organiczny, laser oraz efekty oddziaływania światła z materią. Praca opisująca to doświadczenie została opublikowana w „The Journal of Physical Chemistry Letters”, a grafikę wizualizującą odkrycie umieszczono na okładce tytułowej czasopisma.
W Laboratorium Procesów Ultraszybkich (LPU), które działa na Wydziale Fizyki UW, prowadzone są zaawansowane badania z zakresu optyki laserowej. Pracujący tam naukowcy koncentrują się m.in. na rozwijaniu czułych metod wykorzystujących barwniki organiczne i lasery. Barwniki pobudzane światłem laserowym pozwalają badać różne struktury materiałów biologicznych, takich jak DNA lub białka. Wyniki tych prac mogą znaleźć zastosowanie w diagnostyce genetycznej lub diagnostyce chorób otępiennych. W przyszłości mogą służyć do wczesnego wykrywania tych chorób.
Precyzyjne laserowanie
Doświadczenie przeprowadzone i opisane przez fizyków z LPU polegało na wykorzystaniu metody zwanej laserowaniem. Jest to precyzyjna technika optyczna pozwalająca na wykrycie zmian w strukturze DNA już na poziomie molekularnym.
─ Próbki DNA o określonej strukturze można zsyntezować w warunkach laboratoryjnych. Następnie można je rozpuścić w wodzie i w wyniku zmieszania DNA z barwnikiem organicznym Tioflawiną T badać strukturę DNA. Barwnik Tioflawina T ma szczególne znaczenie, ponieważ jest akceptowalnym przez środowisko medyczne znacznikiem wchodzącym w reakcję z chorobotwórczymi białkami i DNA. W przypadku DNA nici DNA oplatają Tioflawinę T i poprzez zmianę konfiguracji geometrycznej barwnika intensywność świecenia daje nam odpowiedź, czy łączy się z helisą DNA, czy też z fragmentem, który może brać udział w generowaniu chorób. Ta intensywność świecenia wywodzi się ze wzmocnionej emisji spontanicznej, która jest podstawą do zjawiska zwanego laserowaniem ─ tłumaczy dr inż. Piotr Hańczyc z Wydziału Fizyki UW.
Skok intensywności
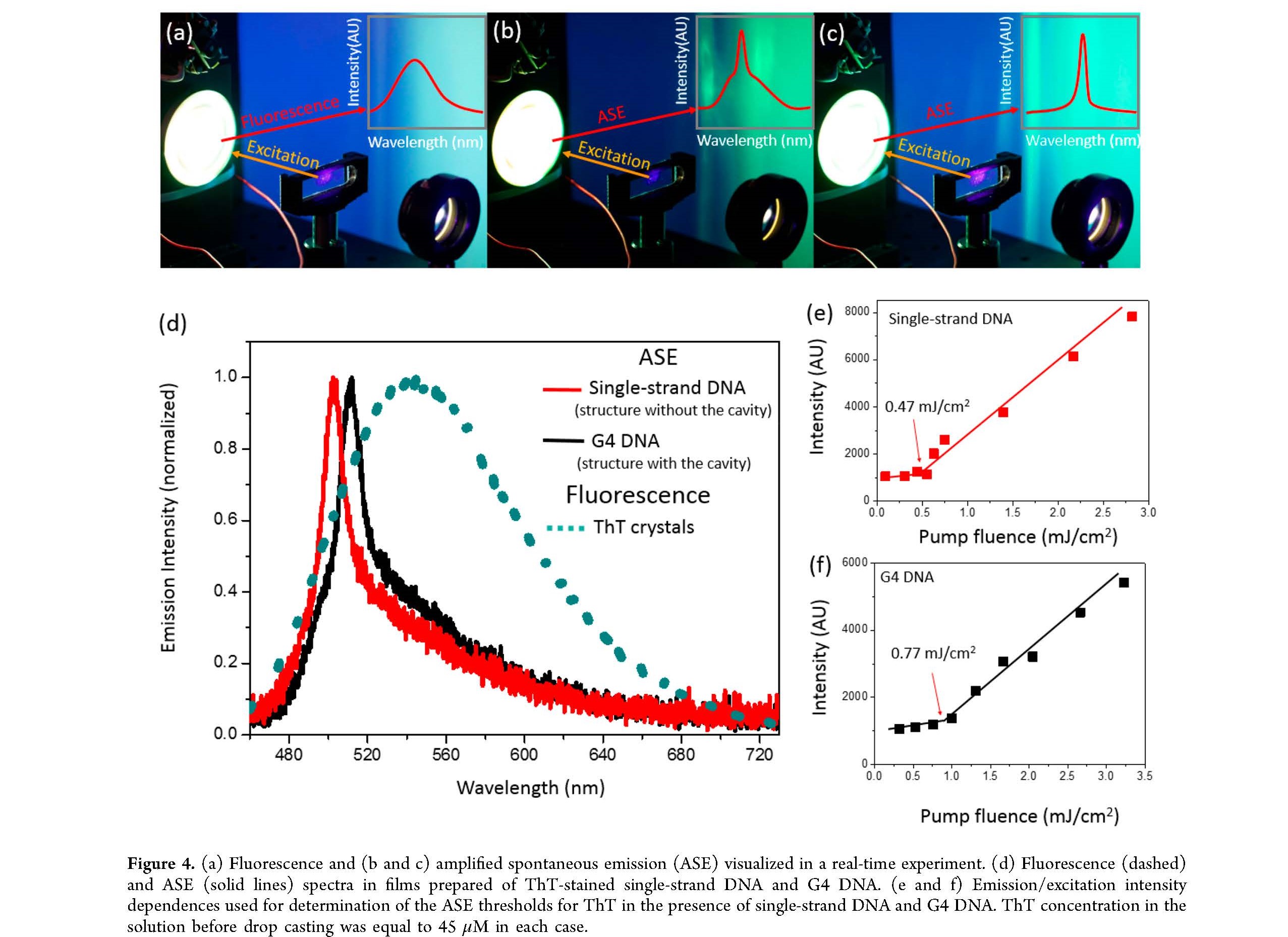
Jak dodaje naukowiec, różnica między zwykłą fluorescencją a zjawiskiem wzmocnionej emisji spontanicznej polega na dużej zmienności intensywności światła emitowanego przez Tioflawinę T związaną z DNA. ─ W eksperymencie najbardziej interesujący jest moment, w którym intensywność świecenia próbki rośnie skokowo. Kontrolując moc lasera świecącego na próbkę sprawdzamy, w którym momencie nastąpi skok intensywności świecenia pochodzący od Tioflawiny T, która oddziałuje z DNA. Nadchodzi wtedy moment tzw. progu generacji wzmocnienia emisji, w którym pojawia się bardzo intensywne świecenie. To właśnie ten próg generacji wzmocnienia emisji w Tioflawinie T jest mocno sprzęgnięty z konkretną strukturą DNA. Próg jest dla nas informacją na temat struktury, z którą barwnik oddziałuje. Dowiadujemy się, czy barwnik łączy się z nicią DNA o prawidłowej budowie, czy też z miejscem potencjalnie chorobotwórczym ─ wyjaśnia dr inż. Piotr Hańczyc.
Prowadzone w LPU prace nad zastosowaniami wzmocnionej emisji spontanicznej w materiałach biologicznych dotyczą nie tylko badań struktury DNA, ale również mechanizmów agregacji białek, które prowadzą do powstawania toksycznych agregatów, tzw. amyloidów, odpowiedzialnych za szereg chorób, w tym choroby Alzheimera i Parkinsona.
Fizycy z UW są też zaangażowani w prace w międzynarodowym konsorcjum pod kierunkiem University of Oxford. Zadaniem naukowców z UW jest opracowanie wczesnych metod wykrywania białek związanych z chorobą Parkinsona. Natomiast konsorcjum pracuje nad szczepionką, która mogłaby zablokować rozwój choroby Parkinsona zanim pojawią się efekty symptomatyczne.
Z pełną treścią artykułu opublikowanego w „The Journal of Physical Chemistry Letters” można zapoznać się tutaj.