Naukowcy z Centrum Nowych Technologii UW oraz Wydziału Fizyki UW pod kierunkiem prof. Jacka Jemielitego i dr hab. Joanny Kowalskiej, we współpracy z badaczami z Instytutu Chemii Fizycznej PAN, opracowali efektywną metodę dostarczania nukleotydów do komórek, która powoduje destrukcję komórek nowotworowych. Rezultaty swoich prac opisali w czasopiśmie naukowym „Chemical Science”.
W artykule “Cellular delivery of dinucleotides by conjugation with small molecules: targeting translation initiation for anticancer applications” opublikowanym w czasopiśmie “Chemical Science” badacze z Centrum Nowych Technologii UW i Wydziału Fizyki UW oraz Instytutu Chemii Fizycznej PAN opublikowali efekty badań prowadzonych pod kierunkiem prof. Jacka Jemielitego i dr hab. Joanny Kowalskiej.
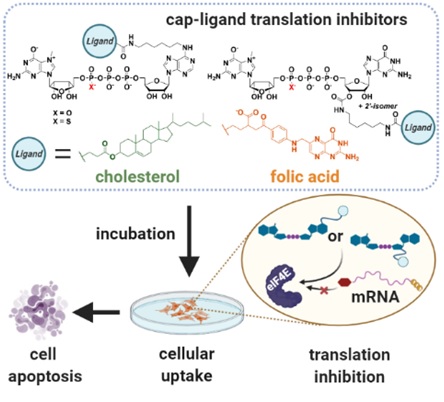
W publikacji po raz pierwszy pokazano, że analogi kapu efektywnie dostarczone do komórek są w stanie zatrzymać proces podziałów komórek nowotworowych, powodując ich destrukcję (zaplanowaną śmierć komórek nowotworowych). Udowodnienie tego było jednym z większych wyzwań w prowadzonych badaniach.
– Udało się ten problem rozwiązać stosując znakowanie fluorescencyjne cząsteczek oraz zaawansowane techniki mikroskopowe, w których specjalizują się badacze z IChF PAN. Te badania to ważny krok w kierunku nowego rodzaju terapii przeciwnowotworowych opartych na analogach końca 5’ mRNA – mówi dr hab. Joanna Kowalska z Wydziału Fizyki UW.
Naukowcy wskazują na szerokie potencjalne możliwości zastosowania opisanej metody. – Metoda zaprezentowana w artykule może mieć charakter ogólny i zostać wykorzystana do dostarczania również innych nukleotydów o potencjale terapeutycznym, co pozwoli na wykorzystanie nukleotydów w leczeniu także innych chorób – podkreśla prof. Jacek Jemielity z CeNT UW.
Dostarczanie nukleotydów do komórek
Nukleotydy są m.in. źródłem energii w komórkach, cząsteczkami wykorzystywanymi do sygnalizacji wewnątrzkomórkowej, jak również międzykomórkowej oraz składnikami kwasów nukleinowych i substratami do ich biosyntezy. Ze względu na swoje niezwykle istotne biologiczne funkcje mają bardzo duży potencjał jako terapeutyki. Polarna budowa tych związków powoduje jednak, że nie są one w stanie wnikać do komórek i nie ma naturalnych mechanizmów komórkowych pozwalających na ich dostarczenie.
Opracowana przez badaczy z UW i PAN metoda polega na łączeniu nukleotydów z niewielkimi cząsteczkami, które mają za zadanie dostarczenie ich do wnętrza komórki. W tym celu naukowcy wykorzystali przede wszystkim cząsteczki cholesterolu, który zapewnia wydajny transport nukleotydów do wnętrza komórek.
Za pomocą tej metody naukowcy wprowadzili do komórek analogi końca 5’ mRNA (analogi kapu) połączone z cząsteczkami cholersterolu. Koniec 5’ mRNA zaangażowany jest w inicjację procesu translacji mRNA, w wyniku czego powstają w komórkach białka. Analogi kapu potrafią naśladować koniec 5’ mRNA, bezpośrednio oddziałując z białkiem eIF4E, co blokuje biosyntezę białka w komórkach.
– Okazuje się, że w wielu nowotworach mamy do czynienia z nadekspresją białka eIF4E, czyli jest go więcej niż w zdrowych komórkach. To powoduje, że translacji zaczynają ulegać białka onkogenne stymulujące proces powstawania nowotworu. Związanie nadmiarowej ilości białka eIF4E może pozwolić na przywrócenie procesu translacji w komórkach na właściwe tory – wyjaśnia prof. Jacek Jemielity.
Pełna treść artykułu dostępna jest pod adresem: https://pubs.rsc.org